Nouvelle publication dans Science pour les équipes Terzi et Pontoglio
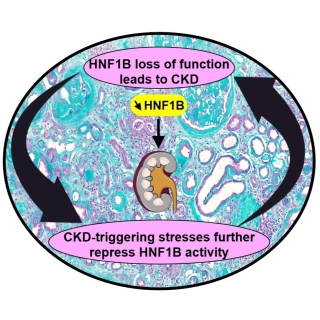
HNF1B intègre des signaux dans une boucle d’amplification qui conduit à la progression des maladies rénales
« HNF1B integrates signals in a feed-forward loop driving kidney disease progression » Science - 16 avril 2026
Les équipes Épigénétique et Développement dirigée par Marco Pontoglio et Mécanismes et stratégies thérapeutiques des maladies rénales chroniques dirigée par Fabiola Terzi à l’INEM, en collaboration avec Katalin Susztak (Université de Pennsylvanie, États-Unis), rapportent l’identification d’un mécanisme moléculaire clé impliqué dans la progression de la Maladie Rénale Chronique, une pathologie qui touche plus de 10 % de la population mondiale.
Initié par Pierre Isnard et Parla Makinistoglu, cette étude publiée dans Science, s’intéresse au rôle du facteur de transcription HNF1B, connu pour sa fonction essentielle lors du développement du rein. À l’aide de modèles murins et de données humaines, ils montrent que la perte d’activité de HNF1B dans les cellules épithéliales tubulaires rénales entraîne une Maladie Rénale Chronique rapide et sévère, caractérisée par une atrophie tubulaire, une fibrose, une inflammation et une insuffisance rénale progressive.
Sur le plan mécanistique, le manque de HNF1B perturbe l’identité des cellules épithéliales et déclenche une réentrée inappropriée dans le cycle cellulaire de cellules tubulaires normalement quiescentes. Cela induit un stress de réplication, des dommages à l’ADN et une mort cellulaire qui contribuent à la dégénérescence tissulaire et à la fibrose. En s’y intéressant de plus près, les auteurs identifient une signature transcriptionnelle dépendante de HNF1B qui est supprimée très précocement dans plusieurs modèles de lésions rénales, avant même l’apparition de lésions détectables.
L’étude montre également que des facteurs associés à la Maladie Rénale Chronique, tels que l’inflammation ou l’albuminurie, limitent activement l’activité de HNF1B via des mécanismes épigénétiques. L’analyse de près de 900 biopsies rénales humaines confirme que la diminution de l’activité de HNF1B est fortement corrélée à la sévérité de la maladie, reliant ce mécanisme à un large éventail de pathologies rénales.
Dans leur ensemble, ces résultats mettent en évidence l’existence d’une boucle d’amplification auto-entretenue dans laquelle la perte de HNF1B favorise la maladie rénale, tandis que les stress associés à la maladie suppriment davantage son activité. La compréhension de ce mécanisme permet de relier les maladies rénales génétiques rares aux formes plus communes de Maladie Rénale Chronique et identifie HNF1B comme une cible thérapeutique potentielle pour ralentir ou modifier la progression de la maladie.
🔗 Click here to access the article
Crédits image : Marco Pontoglio